1- Demostrar experimental algunas de las diferencias de los compuestos orgánicos e inorgánicos.
Introducción
Los primeros químicos establecieron una distinción entre los compuestos que constituyen las rocas y los suelos; los compuestos que se originan durante el crecimiento de las plantas y de los animales. Bajo este punto de vista estos últimos se forman por medio de una fuerza vital asociada con el proceso de la vida su síntesis en el laboratorio era imposible. De acuerdo con esto se les llamo compuestos orgánicos, diferenciarlos de dichos compuestos minerales, a los cuales se les llamo compuestos inorgánicos.
La gama de compuestos orgánicos ( compuestos del carbono) es realmente extensa , es por esto que este laboratorio el cual es una pequeña introducción se basara principalmente en tratar como están conformados dichos compuestos y el sus formas alotrópicas y esencialmente de dar a conocer la química orgánica desde el compuesto carbono, sus formas , reaccione y aleaciones con y respecto a otros elementos en la naturaleza.
Materiales y Reactivos
1- Gradilla de Tubos de ensayo:
Es una herramienta que forma parte del material de laboratorio (química) y es utilizada para sostener y almacenar gran cantidad de tubos de ensayo,de todos los diámetros y formas.Su principal función es facilitar el manejo de los tubos de ensayo. Normalmente es utilizado para sostener y almacenar este material. Este se encuentra hecho de madera, plástico o metal; pero las mas comunes son las de madera.

2- Vaso precipitado de de 100 y 200 ml:
Es un material de laboratorio de vidrio que se utiliza para contener sustancias, disolverlas, atacarlas, calentarlas y en general cualquier cosa que no necesite una medida de precisión del volumen.
Existen varios tamaños de vasos de precipitados, desde muy pequeños que suelen tener un volumen aproximado de 1mL hasta varios litros. Los más comunes son los de 250 y 500 ml. Aún que tenga divisiones marcadas (por ejemplo un vaso de 250 mL, tendrá divisiones en 50, 100, 150, 200 y 250 ml) por el fabricante, estas marcas son sólo aproximadas y se deben de tomar como una referencia, ya que el vaso de precipitados no tiene la función de medir con precisión el volumen.

3- Soporte Universal con Anillo:
Es un utensilio de hierro que permite sostener varios recipientes.
Es un utensilio de hierro que permite sostener varios recipientes.

4- Termómetro:
es un instrumento de medición de temperatura. Desde su invención ha evolucionado mucho, principalmente a partir del desarrollo de los termómetros electrónicos digitales.
es un instrumento de medición de temperatura. Desde su invención ha evolucionado mucho, principalmente a partir del desarrollo de los termómetros electrónicos digitales.

5- Alambre de Asbesto:
Es una tela de alambre de forma cuadrangular con la parte central recubierta de asbesto, con el objeto de lograr una mejor distribución del calor.
Se utiliza para sostener utensilios que se van a someter a un calentamiento y con ayuda de este utensilio el calentamiento se hace uniforme.

6- Pinzas para tubos de Ensayo:
Permiten sujetar tubos de ensayo y si éstos se necesitan calentar, siempre se hace sujetándolos con estas pinzas, esto evita accidentes como quemaduras.
Permiten sujetar tubos de ensayo y si éstos se necesitan calentar, siempre se hace sujetándolos con estas pinzas, esto evita accidentes como quemaduras.
7- Pipetas Graduadas de 5 y 20 ml:
Es un instrumento volumétrico de laboratorio que permite medir alícuota de líquido con bastante precisión. Suelen ser de vidrio. Está formada por un tubo transparente que termina en una de sus puntas de forma cónica, y tiene una graduación (una serie de marcas grabadas) indicando distintos volúmenes.
Es un instrumento volumétrico de laboratorio que permite medir alícuota de líquido con bastante precisión. Suelen ser de vidrio. Está formada por un tubo transparente que termina en una de sus puntas de forma cónica, y tiene una graduación (una serie de marcas grabadas) indicando distintos volúmenes.

8- Espátula:
es una herramienta que consiste en una lámina plana de metal con agarradera o mango similar a un cuchillo con punta roma. uno de los materiales de laboratorio. Se utiliza para tomar pequeñas cantidades de compuestos reactivos que son básicamente polvo. Se suele clasificar dentro del material de metal y es común encontrar en recetas técnicas el término punta de espátula para referirse a esa cantidad aproximadamente.
es una herramienta que consiste en una lámina plana de metal con agarradera o mango similar a un cuchillo con punta roma. uno de los materiales de laboratorio. Se utiliza para tomar pequeñas cantidades de compuestos reactivos que son básicamente polvo. Se suele clasificar dentro del material de metal y es común encontrar en recetas técnicas el término punta de espátula para referirse a esa cantidad aproximadamente.

9- Balanza:
es un instrumento utilizado en el laboratorio, que sirve para medir la masa. Su característica más importante es que poseen muy poca incertidumbre, lo que las hace ideales para utilizarse en mediciones muy precisas.
Las balanzas analíticas generalmente son digitales, y algunas pueden desplegar la información en distintos sistemas de unidades. Por ejemplo, se puede mostrar la masa de una sustancia en gramos, con una incertidumbre de 0,00001g. (0,01 mg).

Reactivos
Cloruro de Sodio: es un compuesto químico con la fórmula NaCl. El cloruro de sodio es una de las salesresponsable de la salinidad del océano y del fluido extracelular de muchos organismos. También es el mayor componente de la sal comestible, es comúnmente usada como condimento y conservante de comida.
General | |
|---|---|
| Nombre | Cloruro sódico |
| Fórmula química | NaCl |
| Apariencia | sólido blanco o claro |
Físicas | |
| Peso molecular | 58,4 uma |
| Punto de fusión | 1074 K (801 °C) |
| Punto de ebullición | 1738 K (1465 °C) |
| Densidad | 2,2 ×103 kg/m3 |
| Estructura cristalina | f.c.c. |
| Solubilidad | 35,9 g en 100g de agua |
Termoquímica | |
| ΔfH0gas | -181,42 kJ/mol |
| ΔfH0líquido | -385,92 kJ/mol |
| ΔfH0sólido | -411,12 kJ/mol |
| S0gas, 1 bar | 229,79 J·mol-1·K-1 |
| S0líquido, 1 bar | 95,06 J·mol-1·K-1 |
| S0sólido | 72,11 J·mol-1·K-1 |
Riesgos | |
| Ingestión | Peligroso en grandes cantidades |
| Inhalación | Puede causar irritación |
| Piel | Puede causar irritación |
| Ojos | Puede causar irritación |
| Más información | Hazardous Chemical Database (En inglés) |
En condiciones normales de presión y temperatura salvo que se indique lo contrario. ATENCIÓN: El apartado de seguridad se incluye únicamente a título informativo. Recuerde que los productos químicos han de manejarse con las debidas precauciones y siguiendo las indicaciones de la ficha de seguridad y el etiquetado del producto. Exenciones y referencias </font> </th></tr> </table> El cloruro sódico, NaCl (sal de mesa), de fórmula NaCl, es un compuesto iónico, formado por un catión Na+ (ión sodio) y un anión Cl- (ión cloruro), el NaCl es el producto de una reacción violenta en la cual un átomo de Na (metal reactivo) reacciona con uno de Cl (un no metal). <p>2Na + Cl2 → 2NaCl nota: se necesitan dos átomos de Na, porque el Cl se encuentra como molécula diatómica en la naturaleza. En la reacción, dos átomos de Na se oxidan cediendo cada uno su único e- (electrón) de valencia a los átomos de Cl, esto se representa como sigue: | |
Ambos átomos, tanto los de Na como los de Cl, cumplen con la regla del octeto. </dt> | |
|---|---|
Nitrato de Potasio: El compuesto químico nitrato de potasio, componente del salitre, nitrato potásico o nitrato de potasa es un nitrato cuya fórmula es KNO3. Actualmente, la mayoría del nitrato de potasio viene de los vastos depósitos de nitrato de sodio en los desiertos Chilenos. El nitrato de sodio es purificado y posteriormente se le hace reaccionar en una solución con cloruro de potasio (KCl), en la cual el nitrato de potasio, menos soluble, cristaliza.
Nitrato de potasio | |||
| |||
| Nombre (IUPAC) sistemático | |||
|---|---|---|---|
| Trioxonitrato (V) de potasio | |||
| General | |||
| Otros nombres | Nitrato de potasio Nitrato potásico Nitrato de potasa Salitre | ||
| Fórmula semidesarrollada | KNO3 | ||
| Fórmula molecular | KNO3 | ||
| Identificadores | |||
| Número CAS | 7757-79-1 | ||
| Número RTECS | TT3700000 | ||
| Propiedades físicas | |||
| Estado de agregación | Sólido | ||
| Apariencia | blanco o gris sucio | ||
| Densidad | 2100 kg/m3; 2,1 g/cm3 | ||
| Masa molar | 101,103 g/mol g/mol | ||
| Punto de fusión | 607 K (334 °C) | ||
| Punto de ebullición | 673 K (400 °C) | ||
| Estructura cristalina | Ortorrómbico, Aragonita | ||
| Propiedades químicas | |||
| Solubilidad enagua | 38 g en 100g de agua | ||
| Peligrosidad | |||
| NFPA 704 | |||
| Número RTECS | TT3700000 | ||
| Riesgos | |||
| Ingestión | Puede causar irritación, náusea, vómitos y diarrea. | ||
| Inhalación | Irritación, exposición a largo plazo puede resultar fatal. | ||
| Piel | Bajo riesgo. | ||
| Ojos | Bajo riesgo. | ||
| Valores en el SI y en condiciones normales (0 °C y 1 atm), salvo que se indique lo contrario. Exenciones y referencias | |||
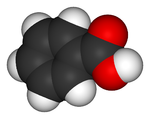
Ácido Benzoico: es un ácido carboxílico aromático que tiene un grupo carboxilo unido a un anillo fenílico. En condiciones normales se trata de un sólido incoloro con un ligero olor característico. Es poco soluble en agua fría pero tiene buena solubilidad en agua caliente o disolventes orgánicos.
Ácido benzoico | |||
| |||
| Nombre (IUPAC) sistemático | |||
|---|---|---|---|
| Ácido benzoico | |||
| General | |||
| Fórmula semidesarrollada | φCOOH | ||
| Fórmula molecular | C6H5-COOH | ||
| Identificadores | |||
| Número CAS | 65-85-0 | ||
| Propiedades físicas | |||
| Densidad | 1320 kg/m3; 1,32g/cm3 | ||
| Masa molar | 122,12 g/mol | ||
| Punto de fusión | 395 K (121,85 °C) | ||
| Punto de ebullición | 522 K (248,85 °C) | ||
| Propiedades químicas | |||
| Solubilidad en agua | 3,4 g/l a 293 K (20°C) 70 g/l a 368 K (95 °C) | ||
| Riesgos | |||
| LD50 | 1.700 mg/kg (rata) LDLo: 500 mg(hombre) | ||
| Valores en el SI y en condiciones normales (0 °C y 1 atm), salvo que se indique lo contrario. Exenciones y referencias | |||
Almidón: El almidón es un polisacárido de reserva alimenticia predominante en las plantas, constituido por amilosa y amilopectina. Proporciona el 70-80% de las calorías consumidas por los humanos de todo el mundo. Tanto el almidón como los productos de la hidrólisis del almidón constituyen la mayor parte de los carbohidratos digestibles de la dieta habitual. Del mismo modo, la cantidad de almidón utilizado en la preparación de productos alimenticios, sin contar el que se encuentra presente en las harinas usadas para hacer pan y otros productos de panaderia. Los almidones comerciales se obtienen de las semillas de cereales, particularmente de maíz (Zea mays), trigo (Triticum spp.), varios tipos de arroz (Oryza sativa), y de algunas raíces y tubérculos, particularmente de patata (Solanum tuberosum), batata (Ipomoea batatas) y mandioca (Manihot esculenta). Los almidones modificados tienen un número enorme de posibles aplicaciones en los alimentos, que incluyen las siguientes: adhesivo, ligante, enturbiante, formador de películas, estabilizante de espumas, agente anti-envejecimiento de pan, gelificante, glaseante, humectante, estabilizante, texturizante y espesante.
El almidón se diferencia de todos los demás carbohidratos en que, en la naturaleza se presenta como complejas partículas discretas (gránulos). Los gránulos de almidón son relativamente densos, insolubles y se hidratan muy mal en agua fría. Pueden ser dispersados en agua, dando lugar a la formación de suspensiones de baja viscosidad que pueden ser fácilmente mezcladas y bombeadas, incluso a concentraciones mayores del 35%.
Benceno | |||
| |||
| Nombre (IUPAC) sistemático | |||
|---|---|---|---|
| 1,3,5-Ciclohexatrieno | |||
| General | |||
| Otros nombres | Benzol | ||
| Fórmula semidesarrollada | C6H6 | ||
| Fórmula molecular | n/d | ||
| Identificadores | |||
| Número CAS | 71-43-2 | ||
| Número RTECS | CY1400000 | ||
| Propiedades físicas | |||
| Estado de agregación | Líquido | ||
| Apariencia | Incoloro | ||
| Densidad | 878.6 kg/m3; 0,8786g/cm3 | ||
| Masa molar | 78.1121 g/mol | ||
| Punto de fusión | 278.6 K (5,45 °C) | ||
| Punto de ebullición | 353.2 K (80,05 °C) | ||
| Viscosidad | 0.652 | ||
| Propiedades químicas | |||
| Solubilidad en agua | 1.79 | ||
| Momento dipolar | 0 D | ||
| Compuestos relacionados | |||
| Hidrocarburos | Ciclohexano Naftaleno | ||
| Termoquímica | |||
| ΔfH0gas | 82.93 kJ/mol | ||
| ΔfH0líquido | 48.95 kJ/mol | ||
| S0líquido, 1 bar | 150 J·mol-1·K-1 | ||
| Peligrosidad | |||
| Punto de inflamabilidad | 262 K (-11 °C) | ||
| NFPA 704 | |||
| Temperatura de autoignición | 834 K (561 °C) | ||
| Número RTECS | CY1400000 | ||
| Valores en el SI y en condiciones normales (0 °C y 1 atm), salvo que se indique lo contrario. Exenciones y referencias | |||
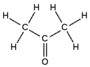
La acetona o propanona: es un compuesto químico de fórmula química CH3(CO)CH3 del grupo de las cetonas que se encuentra naturalmente en el medio ambiente. A temperatura ambiente se presenta como un líquido incoloro de olor característico. Se evapora fácilmente, es inflamable y es soluble en agua. La acetona sintetizada se usa en la fabricación de plásticos, fibras, medicamentos y otros productos químicos, así como disolvente de otras sustancias químicas.
Acetona | |||
| |||
| Nombre (IUPAC) sistemático | |||
|---|---|---|---|
| Propanona | |||
| General | |||
| Otros nombres | Dimetilcetona Acetona ß-cetopropano | ||
| Fórmula semidesarrollada | CH3(CO)CH3 | ||
| Fórmula molecular | C3H6O | ||
| Identificadores | |||
| Número CAS | 67-64-1 | ||
| Número RTECS | AL31500000 | ||
| Propiedades físicas | |||
| Estado de agregación | Líquido | ||
| Apariencia | Incoloro | ||
| Densidad | 790 kg/m3; 0,79 g/cm3 | ||
| Masa molar | 58,04 g/mol | ||
| Punto de fusión | 178.2 K (-94.9 °C) | ||
| Punto de ebullición | 329.4 K (56.3 °C) | ||
| Viscosidad | 0,32 cP a 20 °C (293 K) | ||
| Índice de refracción | 1.35900 (20 °C) | ||
| Propiedades químicas | |||
| Solubilidad enagua | Soluble. También puede disolverse en etanol,isopropanol y tolueno | ||
| Momento dipolar | 2,91 D | ||
| Compuestos relacionados | |||
| cetonasrelacionadas | Butanona | ||
| Otros compuestos relacionados | Propano Propanal Ácido propílico | ||
| Peligrosidad | |||
| Punto de inflamabilidad | 253 K (-20 °C) | ||
| NFPA 704 | |||
| Temperatura de autoignición | 738 K (465 °C) | ||
| Frases R | R11, R36, R66, R67 | ||
| Frases S | S2, S9, S16, S26 | ||
| Número RTECS | AL31500000 | ||
| Riesgos | |||
| Ingestión | Náuseas, vómitos (para mayor información, véase Inhalación). | ||
| Inhalación | Salivación, confusión mental, tos, vértigo, somnolencia, dolor de cabeza, dolor de garganta, pérdida del conocimiento. | ||
| Piel | Piel seca, enrojecimiento. | ||
| Ojos | Enrojecimiento, dolor, visión borrosa. Posible daño en la córnea. | ||
| LD50 | >2000 mg/kg, oral (en ratas) | ||
| Valores en el SI y en condiciones normales (0 °C y 1 atm), salvo que se indique lo contrario. Exenciones y referencias | |||
Ácido Sulfúrico: es un compuesto químico muy corrosivo cuya fórmula es H2SO4. Es el compuesto químico que más se produce en el mundo, por eso se utiliza como uno de los tantos medidores de la capacidad industrial de los países. Una gran parte se emplea en la obtención de fertilizantes. También se usa para la síntesis de otros ácidos y sulfatos y en la industria petroquímica.
Ácido sulfúrico | |||
| |||
| Nombre (IUPAC) sistemático | |||
|---|---|---|---|
| Ácido tetraoxosulfúrico (VI) | |||
| General | |||
| Otros nombres | Tetraoxosulfato (VI) de hidrógeno Aceite de vitriolo Licor de vitriolo Espíritu de vitriolo | ||
| Fórmula semidesarrollada | H2SO4 | ||
| Fórmula molecular | n/d | ||
| Identificadores | |||
| Número CAS | 7664-93-9 | ||
| Propiedades físicas | |||
| Estado de agregación | Líquido | ||
| Apariencia | Líquido aceitoso incoloro (PURO) o líquido aceitoso ambarino (si NO es PURO) | ||
| Densidad | 1800 kg/m3; 1.8 g/cm3 | ||
| Masa molar | 98,08 g/mol | ||
| Punto de fusión | 283 K (10 °C) | ||
| Punto de ebullición | 610 K (337 °C) | ||
| Propiedades químicas | |||
| Acidez (pKa) | pKa1 = -6.62 pKa2 = 1.99 | ||
| Solubilidad enagua | Miscible | ||
| Termoquímica | |||
| ΔfH0líquido | -814 kJ/mol | ||
| S0líquido, 1 bar | 19 J·mol-1·K-1 | ||
| Peligrosidad | |||
| NFPA 704 | |||
| Valores en el SI y en condiciones normales (0 °C y 1 atm), salvo que se indique lo contrario. Exenciones y referencias | |||
Sacarosa: Es un disacárido que no tiene poder reductor sobre el reactivo de Fehling y el reactivo de Tollens.
El azúcar de mesa es el edulcorante más utilizado para endulzar los alimentos y suele ser sacarosa. En la naturaleza se encuentra en un 20% del peso en la caña de azúcar y en un 15% del peso de la remolacha azucarera, de la que se obtiene el azúcar de mesa. La miel también es un fluido que contiene gran cantidad de sacarosa parcialmente hidrolizada.Sacarosa | |
| Nombre (IUPAC) sistemático | |
|---|---|
| n/d | |
| General | |
| Fórmula semidesarrollada | β-D-fructofuranosil-(2<->1)-α-D-glucopiranósido |
| Fórmula molecular | C12H22O11 |
| Identificadores | |
| Número CAS | 57-50-1 |
| Propiedades físicas | |
| Estado de agregación | sólido |
| Apariencia | cristales blancos |
| Densidad | 1587 kg/m3; 1.587 g/cm3 |
| Masa molar | 342,29648 g/mol g/mol |
| Punto de fusión | 459 K (185,85 °C) |
| Punto de descomposición | 459 K ( °C) |
| Propiedades químicas | |
| Acidez (pKa) | 12,62 |
| Solubilidad enagua | 203,9 g/100 ml (293K) |
| Valores en el SI y en condiciones normales (0 °C y 1 atm), salvo que se indique lo contrario. Exenciones y referencias | |








No hay comentarios:
Publicar un comentario